FDA 已接受审评 Keytruda 的sBLA申请,用于治疗晚期或转移性尿路上皮癌——Keytruda可显著延长患者总生存期
默沙东公司随之宣布,FDA 已接受审评 Keytruda的两个补充生物制剂许可证申请(sBLA),用于治疗晚期或转移性尿路上皮癌。其中,一线治疗申请用于治疗不适合含顺铂化疗的患者,二线治疗申请用于治疗含铂化疗时或之后疾病进展的患者。
Keytruda用于晚期尿路上皮癌患者的数据是有希望的
尿路上皮癌是最常见的一种膀胱癌,复发率和进展率都较高。数据统计,约50-70%的患者五年内会复发。但一直以来该癌症的二线治疗方案非常有限,不少制药巨头一直谋求行之有效的免疫肿瘤治疗方案。
默沙东公司的底气,就来自于2期Keytruda-052 试验和3期Keytruda-045 试验数据都比较亮眼。其中,Keytruda-045 是一项随机研究,评估的正是Keytruda 相对于化疗是否对治疗晚期或转移性尿路上皮癌更有效。
实验中,542例晚期尿路上皮癌复发或进展后患者,被随机分配分别接受Keytruda(200毫克剂量+每3周一次静脉给药),或化疗药物紫杉醇、多西紫杉醇或长春氟宁治疗,共同终点为总生存率和无进展生存期。结果显示:
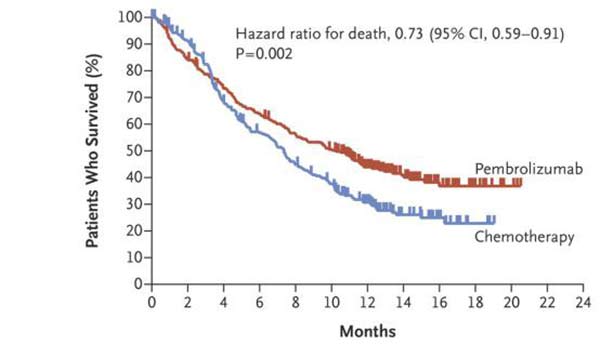
✦Keytruda显著延长患者总生存期。对全部患者而言,Keytruda组中位生存期为10.3个月,化疗组只有7.4个月。
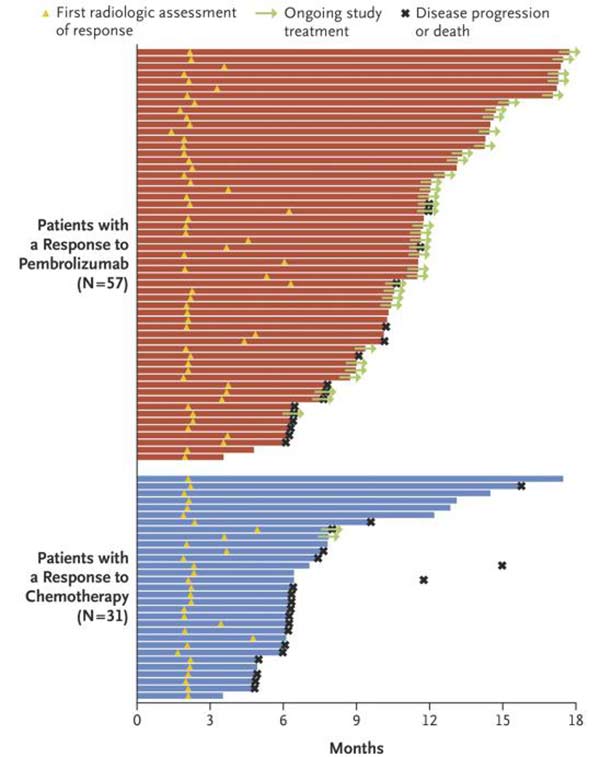
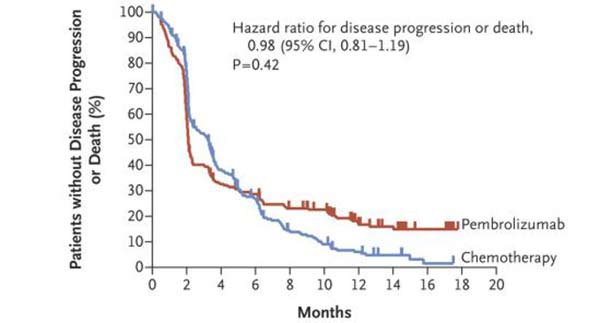
✦Keytruda组与化疗组,在无进展生存期上并没有显著差异,但默沙东公司认为能显著改善总生存期已经足够了。
尿路上皮癌的临床好消息频传,除了默沙东的Keytruda,老对手施贵宝的 Opdivo也被FDA批准用于治疗晚期或转移性尿路上皮癌。Opdivo的推荐剂量为240mg,每两周静脉给药,疗效一样较显著。康安途一直追踪跟进PD-1抑制剂类药物对包括非小细胞肺癌和膀胱癌在内的临床研究,可以预见,PD-1抑制剂应该还有更多“捷报”在后头。

Joaquim Bellmunt et al., Pembrolizumab as Second-Line Therapy for Advanced Urothelial Carcinoma. N Engl J Med,2017.
Nick Mulcahy, In NEJM: Practice-changing trial in urothelial cancer, Medscape, 2017.










请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)