去年8月,PD-1单抗Opdivo在一项代号为“CheckMate 026”的非小细胞肺癌(NSCLC)三期临床试验中意外失败,直接拖累BMS股价大幅下滑。但根据刚刚召开的AACR 2017大会发布的一项最新报告,研究人员在采用肿瘤突变负荷(TMB)作为标志物对CheckMate 026三期临床试验进行回顾性研究后发现,如果选择TMB作为Opdivo治疗NSCLC的biomarker,能显示出更明显的临床获益。
该研究发现,在TMB高表达的病人中,采用Opdivo进行治疗后,客观缓解率(ORR,47% vs 28%)和无进展生存期(PFS,9.7 vs 5.8个月)均显著优于化疗[1],这一结果让Opdivo成为NSCLC一线用药重燃希望。
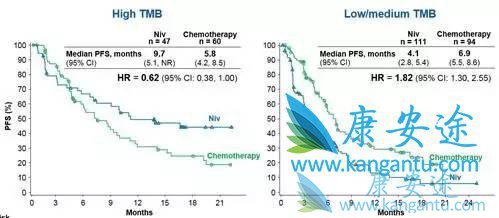
图1 高TMB表达与临床获益显著相关,且优于化疗对照组
要了解这项研究的重要意义,还得从去年Opdivo折戟一线NSCLC治疗的临床试验说起,也不得不提其与老对手默沙东Keytruda相爱相杀的历史。
2016年8月,BMS对外宣布了名为“CheckMate 026”的三期临床试验的核心数据,在PD-L1表达>5%的NSCLC患者中,Opdivo相比化疗,对PFS(4.2 vs 5.9个月)和OS(14.4 vs 13.2个月)都没有显著提高。反观默沙东的Keynote024研究,在PD-L1表达>50%的NSCLC患者中,ORR、PFS甚至OS均完胜化疗,之后也是凭此数据顺利拿下一线治疗NSCLC的适应症。BMS的股价当时一夜之间跌去200亿美元,以惨痛的代价教育后来者PD-L1表达>5%不是一个好的患者入组指标[2]。
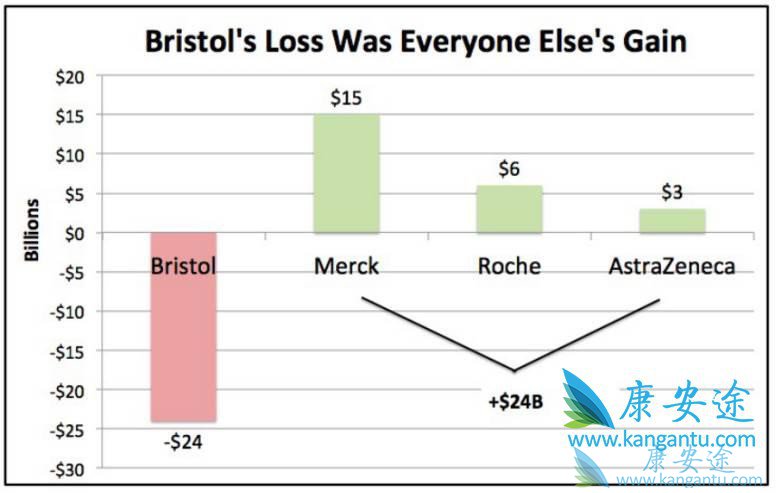
图2 BMS股价暴跌,Merk等股价上涨
2016年10月,在欧洲肿瘤年会上,BMS公布了CheckMate 026的详细数据,结果依旧令人沮丧,即使PD-L1表达>50%的患者,Opdivo的疗效也没有显示优势,股价一天之内又跌了10%[3]。相信此刻BMS的内心是崩溃的,为什么别人家的PD-L1高表达获益这么好?问题究竟出在哪里?
大量的临床前和临床研究显示,Keytruda和Opdivo这两个药物高度相似。在两家公司分别开展的“Keynote 024”和“CheckMate 026”这两项临床试验中,也都是以PD-L1的表达作为入组标准,唯一不同的是Opdivo选择PD-L1>5%作为区分患者的指标,Keytruda选择PD-L1>50%为指标。同为PD-1抑制剂,作用机制也基本相同,且有相似的临床设计,为什么带来了南辕北辙的研究结果?Opdivo当时的这一跤,跌得不明不白。
科学研究容不得侥幸心理,真理也是越辩越明,面对基于PD-1治疗NSCLC的巨大市场,尤其是一线治疗市场,BMS放弃这一领域几乎是不可能的。由于对PD-L1表达检测,本身就存在一些挑战[4-5],在新的回顾性研究中,研究人员认真考虑了所有可能的影响因素。最终,在2017年4月的AACR大会上,新研究探索了在TMB高表达病人中免疫治疗是否优于铂类为基础的化疗,结果得到了肯定!这是第一项分析TMB和PD-1抑制剂的临床获益相关性的重量级III期随机对照研究。这项回顾性研究显示,Opdivo在TMB高表达病人中ORR和PFS结果显著优于铂类为基础化疗。

事实上,此次研究选择TMB作为区分肿瘤免疫治疗获益人群并非一时的误打误撞,而是有着深厚的科学基础。肿瘤是基因突变积累到一定程度引起的疾病,基因突变产生的肿瘤新抗原会被免疫系统识别,进而被免疫系统杀死和清除。TMB负荷越高,肿瘤表达的新抗原越多,被免疫系统识别的可能性也就越大。除了新抗原数量之外,质量也至关重要[6-7]。
如今,国内不少企业在从事TMB与PD-1药物临床疗效关联性的研究,一些领先企业也已经发布了相关产品,比如裕策生物开发的专门针对肿瘤免疫治疗的基因检测产品YuceOneTM,其核心竞争优势就是在对免疫和肿瘤深刻理解的基础上,针对TMB检测从头设计基因panel,测试结果优于国际同行。此外,在上个月,该公司发起了天梯计划[8],以进一步的探索和引领肿瘤精准免疫治疗的方向。针对新抗原发现,AACR墙报#628 Neoantigens predicted by clonal mutationanalysis in lung adenocar-cinoma patients 也展现了其和国内科研机构在neoantigen发现和转化应用上的技术实力。
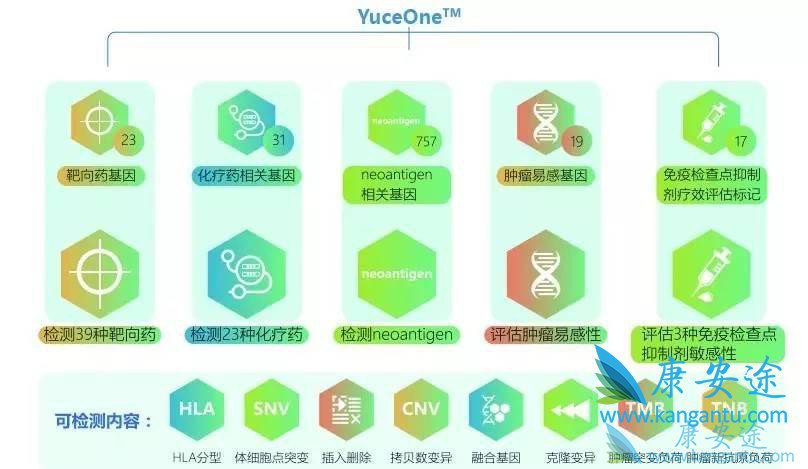
图4 YuceOneTM 检测指标及性能
相比于针对特定基因突变起作用的肿瘤靶向治疗药物,免疫检查点抑制剂疗法代表了完全不同的抗肿瘤机制和疗法。因其对恶性/晚期肿瘤治疗的有效性和多癌种适用性,近年来异常火爆,不断有新的适应症和药物获批。
根据不完全统计,除了已经上市的Yervoy(CTLA-4)、Opdivo(PD-1),Keytruda(PD-1),Tecentriq(PD-L1)之外,全球药物研发管线有数十种免疫检查点抑制剂,国内布局PD-1/PD-L1药物的企业也有数十家。
国内已获批临床的PD-1/PD-L1药物(不完全统计)
根据公开信息显示,誉衡药业、嘉和生物已将TMB纳入其临床试验的检测范围。鉴于AACR大会上对CheckMate 026研究的回顾性分析结果,TMB对可能从免疫检查点抑制剂治疗中获益的患者有更好的区分度,未来应该会有更多药企选择将TMB纳入免疫检查点抑制剂类药物临床试验的检测范围。
参考文献
-
AACR2017.Impact of Tumor Mutation Burden on the Efficacy of First-LineNiv in StageIV or Recurrent Non-Small Cell Lung Cancer:An Exploratory Analysis of CheckMate026.
-
RemonJ,Besse B,Soria JC.Successes and failures: what did we learn from recentfirst-line treatment immunotherapy trials in non-small cell lung cancer? BMCMedicine2017.DOI: 10.1186/s12916-017-0819-3
-
Chemate026余震,施贵宝再跌10%。
-
HirschFR,McElhinny A,Stanforth D,et al.PD-L1 Immunohistochemistry Assays for LungCancer:Results from Phase 1 of the Blueprint PD-L1 IHC Assay ComparisonProject.[J] J Thorac Oncol,2017;12:208–22
-
大叔快评:肺癌PD-L1要不要检测?江湖需要一个统一的声音。
-
RIZVI NA,HELLMANN MD,SNYDER A,etal.Mutational Landscape Determines Sensitivity to Programmed Cell Death-1Blockade in Non-Small Cell Lung Cancer[J].Science,2015,348(6230):124-8.
-
大叔快评:肿瘤突变负荷(TMB)会是下一个bio-marker吗?
-
裕策生物:“天梯计划”助力肿瘤精准免疫治疗










请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)