由于阿达木单抗为AbbVie带来了巨额收入,因此AbbVie非常努力地捍卫阿达木单抗的专利权。Humira专利诉讼战的第一枪于2015年在美国打响,Amgen公司于2015年6月26日针对Abbvie的配方专利US8916157和US8916158向美国专利局双方复审程序(IPR),声称这两项专利不具备新颖性和创造性,这些专利和其他配方专利将于2022年到期。在审查过程中,美国专利局最初以双重专利为由驳回了这组专利。因此,Amgen似乎在这场专利战中取得胜利。此外,鉴于这整套配方专利的高度相似性,撤销两项专利可能会导致撤销剩余专利。
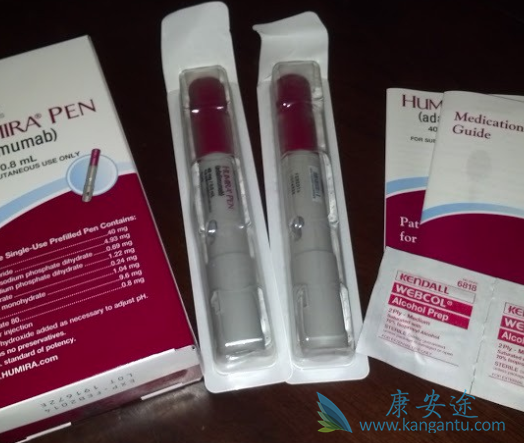
面对Humira的“专利悬崖”,Abbvie除了通过延长Humira的保护期进行防御,还选择了妥协共享市场。三星旗下生物制药公司Samsung Bioepis曾联合其欧洲商业化合作伙伴Biogen提起了专利无效诉讼。2017年3月3日,英国法院做出判决,称艾伯维相关专利申请不存在专利性。然而在2017年4月5日,艾伯维宣布与Samsung Bioepis就阿达木单抗生物类似药的专利侵权诉讼在全球范围内达成和解。除了Samsung Bioepis之外,还有包括Amgen和辉瑞在内的6家制药公司就阿达木单抗生物类似药的专利侵权诉讼达成和解,这些公司的阿达木单抗生物类似药在美国上市时间需等到2023年以后。
尽管Abbvie作出了努力,第一个阿达木单抗生物仿制药已于2016年9月23日获得FDA批准,即Amgen的Amjevitar,随后还有勃林格殷格翰的CYLTEZO和诺华旗下Sandoz生产的Hyrimoz也分别获FDA批准。由于正在进行的专利诉讼,阿达木单抗生物仿制药最早要到2023年才能进入美国市场。在欧洲市场上,目前获得欧盟EMA批准的共有5款阿达木单抗生物仿制药,其中山德士的阿达木单抗生物仿制药Hyrimoz已于2018年10月登陆欧洲市场。









请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)