拜耳制药表示,欧盟委员会已经批准了瑞格菲尼(RESIHANCE)用于之前接受了索拉非尼一线治疗的肝细胞癌成人患者治疗的上市许可。Stivarga是目前首个同时也是唯一一个对于二线肝细胞癌治疗具有明显总生存期改善的药物。这次被批准也标志着瑞格菲尼(RESIHANCE)在5个月内的第三次主要地区的批准,该药物分别在今年的4月份和7月份在美国和日本获准肝细胞癌二线治疗。Stivarga也是欧洲地区近十年来首个批准的肝癌二线治疗药物。
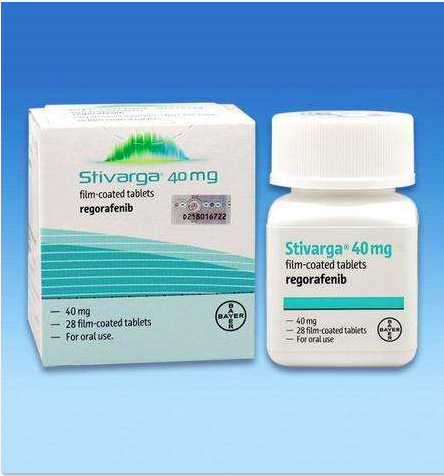
这次欧洲批准是基于一项国际多中心的安慰剂对照临床研究RESORCE的试验数据,这项研究评估了瑞格菲尼(RESIHANCE)用于Nexavar治疗出现疾病进展的肝细胞癌患者的临床有效性。试验结果显示:相比安慰剂联合BSC,regorafenib联合最好的支持疗法(BSC)可以获得具有临床意义的总生存期的显着改善(10.6个月 vs. 7.8个月)(HR 0.63; 95% CI 0.50-0.79; p<0.0001),整个治疗周期内,患者死亡风险降低了37%。RESORCE研究中所观察到的不良事件和瑞格菲尼(RESIHANCE)所知的不良事件相一致,其中最常见的和用药相关的不良反应为手足皮肤反应、腹泻、疲劳和高血压。
详情请访问 瑞格菲尼 https://rgfn.kangantu.com













请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)